PAHの治療方針と実際の治療
- 肺高血圧症では、患者さんが症状を自覚して来院したときはすでに進行している場合が少なくありません。
- したがって、早期診断と早期の治療開始、また症状の重さに応じて十分な治療を行うことが予後の改善につながる可能性は大きいと考えられています。
最新の治療アルゴリズム(第4回肺高血圧症ワールドシンポジウム、2008)
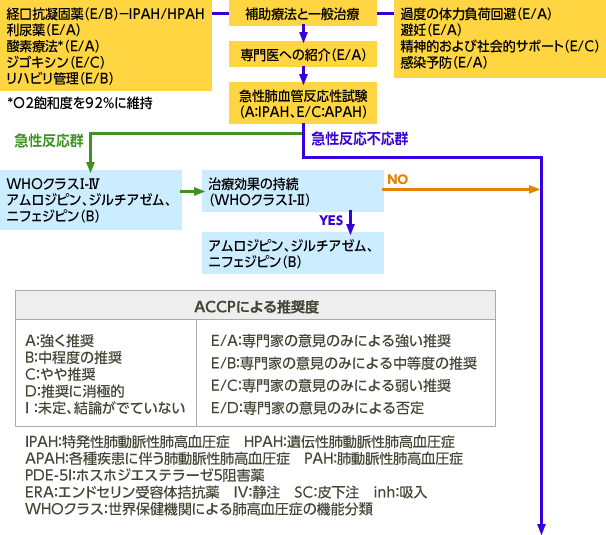
| 推奨度 | WHOクラスⅡ | WHOクラスⅢ | WHOクラスⅣ |
|---|---|---|---|
| A | アンブリセンタン、 ボセンタン、 シルデナフィル | アンブリセンタン、 ボセンタン、 エポプロステノール IV、 アイロプロスト inh、 シルデナフィル | エポプロステノール IV |
| B | シタクセンタン、 タダラフィル | シタクセンタン、 タダラフィル、 トレプロスティニル SC | アイロプロスト inh |
| C | ベラプロスト | トレプロスティニル SC | |
| E/B | アイロプロスト IV、 トレプロスティニル IV | アイロプロスト IV、 トレプロスティニル IV、 初回併用療法(下記参照) | |
| E/C | アンブリセンタン、 ボセンタン、 シルデナフィル、 シタクセンタン、 タダラフィル | ||
| 未承認 | トレプロスティニル inh+ | トレプロスティニル inh+ |
Barst RJ, et al: J Am Coll Cardiol 54: S78-S84, 2009
ガイドラインの治療方針
ガイドラインでは以下のように状態に応じた治療を行うことが推奨されています。
- 抗凝固薬や強心薬、利尿薬などを投与し、その後、血管反応性試験およびWHO機能分類に基づいた治療を行う。
- これらの薬剤の単独治療で効果不十分の場合は、エポプロステノール、エンドセリンおよびホスホジエステラーゼ(PDE)-5阻害薬の組み合わせによる併用療法を行う。
- 十分な効果が得られない場合は肺移植を考慮する。
- PAHの治療はそれぞれの地域における専門医と連携をとって行うことが望ましい。
PAHの治療における効果判定
- PAHの予後因子としては、WHO機能分類、6分間歩行距離、血行動態 (右房圧、心係数)、血中BNPなどが報告されています。そのため、これらの因子はPAHの治療の効果判定や経過観察時の指標として利用されています。
肺動脈性高血圧症の予後決定因子
| 因子 | 低リスク (予後良好) | 高リスク (予後不良) |
|---|---|---|
| 右心不全の兆候 | なし | あり |
| 進行速度 | 緩徐 | 急速 |
| WHO機能分類 | Ⅰ、Ⅱ | Ⅳ |
| 6分間歩行距離 | 長い (400m以上) | 短い (300m以下) |
| 心肺運動負荷検査 | Peak VO2>10.4mL/kg/min | Peak VO2<10.4mL/kg/min |
| 心エコー | 右室機能不全はわずか | 心嚢液、著明な右室拡大/機能不全 |
| 血行動態 | 右房圧<10mmHg、 CI>2.5L/min/m2 | 右房圧>20mmHg、 CI<2.0L/min/m2 |
| BNP | わずかに上昇 | 高度に上昇 |
McLaughlin VV, et al: J Am Coll Cardiol 53: 1573-1619, 2009より改変
薬物療法
| 抗凝固療法 | PAHの肺動脈に微小血栓が存在する場合があることから、PAHに対しては、抗凝固療法としてワルファリンが投与されることが多いです。 |
| Ca拮抗薬 | 治療アルゴリズムでは、急性肺血管反応性試験が陽性であればCa拮抗薬(経口)の投与を行うこととされています。Ca拮抗薬の持続効果がみられるのは、肺動脈性肺高血圧症の患者さんの中でもごく少数ですが、有効である場合には治療効果が大きいことから、診断時に急性血管反応試験を行う施設も多くあります。 |
| PGI2持続静注 | プロスタサイクリン(PGI2)は血管内皮で産生される強力な血管拡張性物質で、これを化学合成した物質がエポプロステノールです。PAH患者さんでは、PGI2合成酵素の産生低下や、血中PGI2の減少と血管収縮物質であるトロンボキサンの相対的な上昇が報告されていることから、体内で不足しているPGI2を補う目的でPGI2持続静注が開発されました。ただしPGI2持続静注療法で投与するPGI2量は内因性PGI2を大きく上回っていること、抗血小板作用や血管平滑筋増殖抑制作用も併せもっていることなどから、従来の血管拡張薬にはない長期的効果が報告されています。PGI2がPAHの生命予後を改善するとの報告は多く、PAH治療の中心的役割を果たしています。 |
| 経口PGI2 誘導体 | PGI2は経口投与ができず、半減期が短いため持続静注をしなければなりません。 そこでPGI2誘導体として経口投与が可能なベラプロストが開発され、2007年には徐放製剤も登場しました。わが国の試験では予後改善効果が得られていますが、欧米では、投与12週後の運動耐容能は改善するものの、1年後には改善効果に有意差がみられないとの報告もあり、使用しているのは日本を含めたいくつかの国に限られています。しかし比較的軽症例には有効であることも多いです。 |
| エンドセリン 受容体拮抗薬 | エンドセリンは、日本人の研究者によって発見された非常に強力かつ持続的な血管収縮作用を持つペプチドです。また内皮細胞の増殖・機能障害作用や線維芽細胞増殖作用、炎症性サイトカイン産生作用など多くの生理作用も有しています。エンドセリン受容体拮抗薬は、そのエンドセリンをブロックして、血管を拡張させます。2005年にボセンタンが、2010年にはアンブリセンタン(いずれも経口薬)が、PAH治療薬として承認されました。 |
| ホスホジエステラーゼ (PDE) -5阻害薬 | NOは血管平滑筋細胞に作用してcGMPを産生し、cGMPが細胞内Ca2+濃度を低下させて血管を拡張します。PDE-5阻害薬は、cGMPを分解するPDE-5の作用を抑制することにより血管を拡張します。2005年にシルデナフィルが、2009年にタダラフィル(いずれも経口薬)が、PAH治療薬として承認されました。 |
| 併用療法 | PAH治療に主に用いられる血管拡張薬は、PGI2、エンドセリン受容体拮抗薬およびPDE-5阻害薬の3系統があります。2~3系統を組み合わせた併用療法が現在試みられており、いずれの組み合わせも効果はあると考えられ、複数の大規模臨床試験が進行中です。 |
PAH治療薬の3つの系統
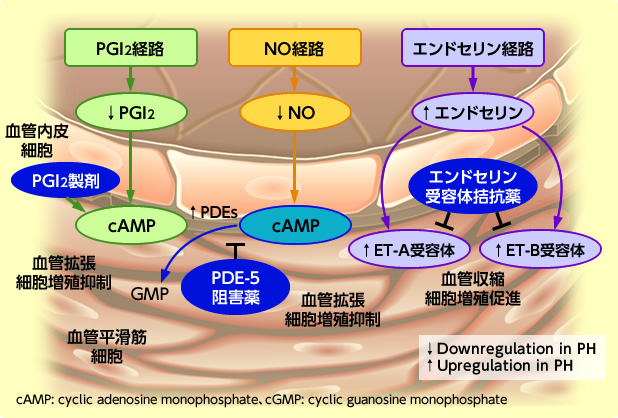
Ghofrani HA, et al: Handbook of Experimental Pharmacology 191: 469-483, 2009より一部改変
エポプロステノール投与で生存率が著しく延長
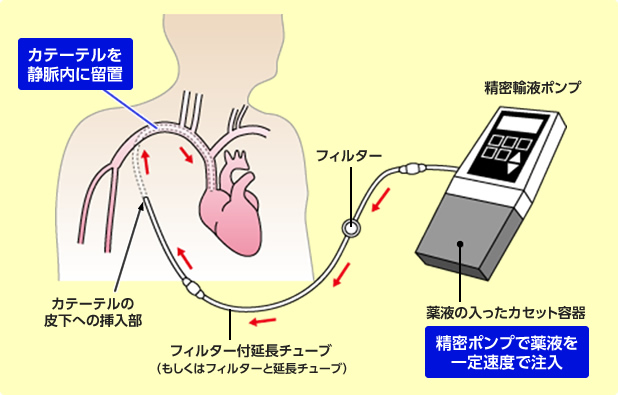
PGI2持続静注(エポプロステノール)は24時間の持続投与が必要であるため、患者さんの負担もある一方、大きな予後改善効果があることが知られており、重症の肺高血圧症の患者さんや、経口薬(飲み薬)だけでは十分な改善効果が得られない患者さんに対して日本では積極的に使用されております。

PGI2持続静注の装置
PAHをターゲットにした治療法における 重要な薬物相互作用
- PAH治療薬の併用療法については本格的な取り組みの機運が高まっており、2009年に発表された欧州心臓学会議:European Society of Cardiology (ESC)/欧州呼吸器学会:European Respiratory Society (ERS)のガイドラインにおいてPAH治療薬の薬物相互作用について具体的に言及されています。
| PAH治療薬 | 相互作用の メカニズム |
相互作用の メカニズム |
相互作用 |
|---|---|---|---|
| アンブリセンタン | ?† | シクロスポリン・ ケトコナゾール |
アンブリセンタンをシクロスポリンおよびケトコナゾールと併用投与する場合は注意が必要である。 |
| ボセンタン | CYP3A4誘導剤 | シルデナフィル | シルデナフィル濃度が50%低下、ボセンタン濃度は50%上昇する。どちらの薬剤も投与量の調整は不要と思われる。 |
| CYP3A4基質 | シクロスポリン | シクロスポリン濃度が50%低下、ボセンタン濃度は4倍になる。併用は禁忌である。 | |
| CYP3A4基質 | エリスロマイシン | ボセンタン濃度が上昇する。短期間の場合はボセンタンの投与量の調整は不要と思われる。 | |
| CYP3A4基質 | ケトコナゾール | ボセンタン濃度が2倍になる。 | |
| CYP3A4基質+胆汁酸塩排泄ポンプ阻害剤 | グリベンクラミド | アミノ基転移酵素濃度が上昇する。グリベンクラミドの血糖低下作用が減弱する可能性がある。併用は禁忌である。 | |
| CYP2C9+CYP3A4基質 | フルコナゾール・ アミオダロン |
ボセンタン濃度がかなり上昇する。併用は禁忌の可能性がある。 | |
| CYP2C9+CYP3A4 誘導剤 |
リファンピシン・ フェニトイン |
ボセンタン濃度が58%低下する。投与量調整の必要性があるかは不明。 | |
| CYP2C9誘導剤 | HMG CoA還元酵素阻害薬 | シンバスタチン濃度が50%低下する。アトルバスタチンでも同様の作用が考えられる。コレステロール値のモニターが必要である。 | |
| CYP2C9誘導剤 | ワルファリン | ワルファリン代謝が増加するので投与量の調整が必要となる可能性がある。ワルファリン開始後にワルファリンについて高度のモニタリングが推奨されているが、投与量の調整は通常は不要である。 | |
| CYP2C9+CYP3A4誘導剤 | ホルモン系避妊薬 | ホルモン値が低下する。避妊が不確実になる。 | |
| シルデナフィル | CYP3A4基質 | ボセンタン | シルデナフィル濃度は50%低下し、ボセンタン濃度は50%上昇する。どちらの薬剤も投与量の調整は不要と思われる。 |
| CYP3A4基質 | HMG CoA還元酵素阻害薬 | 競合代謝によりシンバスタチン/アトルバスタチン濃度が増加する可能性がある。シルデナフィル濃度が高まる可能性がある。横紋筋融解症の危険性が高まる可能性がある。 | |
| CYP3A4基質 | HIVプロテアーゼ阻害薬 | リトナビルとサキナビルはシルデナフィル濃度を著しく高める。シルデナフィルの投与量の調整が通常必要である。 | |
| CYP3A4誘導剤 | フェニトイン | シルデナフィル濃度が低下する可能性がある。 | |
| CYP3A4基質 | エリスロマイシン | シルデナフィル濃度が上昇するが、短期間なら投与量の調整は不要と思われる。 | |
| CYP3A4基質 | ケトコナゾール | シルデナフィル濃度が上昇するが、投与量の調整は不要と思われる。 | |
| CYP3A4基質 | シメチジン | シルデナフィル濃度が上昇するが、投与量の調整は不要と思われる。 | |
| cGMP | 硝酸薬ニコランジル | 重篤な低血圧症が顕著になる。併用は禁忌である。 | |
| タダラフィル | CYP3A4基質 | ボセンタン | 血漿中タダラフィル濃度が42%低下するが、ボセンタン濃度には有意な変化はない。 投与量の調整は不要と思われる。 |
| cGMP | 硝酸薬ニコランジル | 重篤な低血圧症が顕著になる。併用は禁忌である。 |
* † 原文のまま表記しています。
cGMP:環状グアノシン一リン酸、OATP:有機アニオントランスポータータンパク質
Galie N, et al: Eur Heart J 30: 2493-2537, 2009
PAHに対する肺移植の適応基準
薬物療法を十分行っていても改善経過が思わしくない肺高血圧症の患者に対しては、肺移植登録が勧められます。以下は薬物治療を十分行った上での状態からみた、移植適応の国際基準です。ただし、国によって移植までの待機期間は異なり、特に日本では待機期間が長いことから、主治医よりより早期に移植が勧められることもあります。
- NYHA機能分類:Ⅲ~Ⅳ
- 中心静脈圧:>15mmHg
- 平均肺動脈圧:>55mmHg
- 心係数:<2.0L/min/m2
Orens JB, et al: J Heart Lung Transplant 25: 745-755, 2006より作表
